Járványügyi szakértő: A remdesivir hazai gyógyszervizsgálata alkalmatlan a gyógyszer vizsgálatára
(A szerző klinikai biostatisztikus, orvosbiológiai mérnök, az Óbudai Egyetem habilitált egyetemi docense. Az írás saját nézeteit tükrözi, nem hivatalos állásfoglalása az előbbi szervnek.)
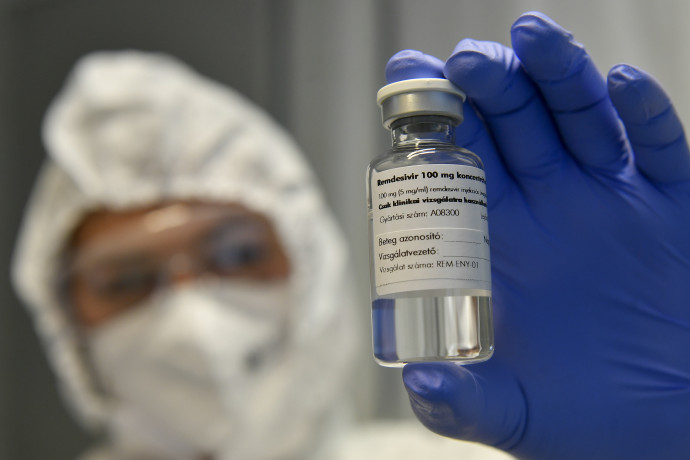
Nemrégiben megkezdődött az egyik legígéretesebb koronavírus elleni gyógyszer, a remdesivir hazai gyógyszervizsgálata. Ez hatalmas, nemzetközi szinten is említésre méltó eredmény – nem csak a gyógyszer hazai legyártása, de önmagában a klinikai vizsgálat is. A tervek szerint kétezer beteget vonnak be a kutatásba. Érzékeltetni is nehéz ennek a súlyát: a világ egyik legnagyobb tekintélyű orvosi folyóiratában, a New England Journal of Medicine-ben pár héttel ezelőtt megjelent remdesivir-vizsgálat végleges eredménye, ami már most az egyik alapvető forrása az erről szóló tudásunknak, összesen 1062 alanyt vont be. A magyar vizsgálat ennek kétszeresét célozza meg.
Ennek megvalósítása rendkívüli siker lenne a hazai egészségügynek, és a magyar orvosi kutatásoknak is. Minden pátosz nélkül mondhatom, egy ilyen vizsgálat sikeres végrehajtása nem csak a kutatók, de érdeklődő laikusok százmilliói számára rakná fel Magyarországot a térképre. Szeretném, ha az olvasó megértené, hogy itt annál sokkal többről van szó, mint hogy a magyar betegek kezeléséhez jobb információnk lesz (pedig már ez is hatalmas eredmény): egy ilyen vizsgálat érdemben hozzájárulhatna az emberiség orvosi tudásához, mégpedig egy példátlan népegészségügyi jelentőségű kérdésben, és a mindennapi gyakorlatban közvetlenül hasznosítható módon. Nem tudom, ilyet magyar földön végrehajtott vizsgálat kapcsán milyen sűrűn lehet leírni.
Mindezek fényében különösen sajnálatos, hogy a vizsgálatot olyan módon tervezték meg, ami lényegében garantálja, hogy semmilyen használható információ ne derülhessen ki azokról a kérdésekről, amik a legfontosabbak lennének a remdesivir kapcsán.
Ez elég sokkolóan hangozhat első olvasásra, de ha ez így van, akkor kritikusan fontos, hogy erről a magyar közvélemény értesüljön.
A véleményem megfogalmazásához az európai gyógyszerhatóság kutatás-regiszterébe leadott rövid összefoglalót használtam. Hogy miért csak ezt a minimálisan kötelező közlendőt, és nem valamilyen részletesebb leírást? Nos, ezzel el is érkeztünk a problémák kezdetéhez…
Nulladik probléma: a 100%-ban közpénzből finanszírozott vizsgálat protokollja nem nyilvános
Egy klinikai vizsgálat esetében protokollnak szokás nevezni a kutatás részletes tervét. A protokoll dokumentálja a vizsgálat konkrét célját, a vizsgálat megtervezésének minden aspektusát a bevonandó betegek körétől a létszámukon át a vizsgált kimenetekig, tartalmazza a lefolytatás forgatókönyvét, a kiértékelés menetét, statisztikai módszereit, és egy egész sor technikai kérdést meghatároz.
Ha valaki utána akar nézni a remdesivir hazai vizsgálatának, itt rögtön belefut egy problémába: nem fogja megtalálni a kutatás protokollját. Nem csak valamiféle véletlenről van szó: a kutatást koordináló konzorcium, a Hungarian Clinical Research Infrastructure Network szerint a protokoll „védett szellemi termék”, ezért szándékosan nem publikus.
(Egy kiegészítő megjegyzést hadd tegyek ezen a ponton. Mielőtt ezt a cikket megírtam volna, természetesen először megpróbáltam a „hivatali utat” követni, és a nyilvánosság bevonása nélkül tisztázni a kérdéseimet. A konzorcium vezetője megírta, hogy a protokoll nem nyilvános, a további kérdésemet illetően válaszra sem méltatott. A későbbi felvetésemre, hogy ha nagyon elfoglalt, irányítson el máshoz, aki tud segíteni, szintén nem válaszolt; ezt követően megpróbáltam felvenni a kapcsolatot az összefoglaló „kapcsolattartó további információkért” pontjában megadott hölggyel, de itt sem jártam sikerrel, kereken közölte, hogy az összefoglalón túl sajnos nem áll módjában több információt adni. Mindebben nem az én szerepem az érdekes, – nyilvánvaló, hogy ezek után nem hőstett, hanem erkölcsi minimum-kötelesség a nyilvánossághoz fordulni, ha már más utat nem hagytak – inkább az, hogy ha én így jártam, egyetemi címmel, teljes titulusommal a levélben, akkor vajon egy átlagember érdeklődőnek mennyi esélye lett volna bármilyen kommunikációra a vizsgálatot megtervezőkkel.)
Bár mindezek jogilag biztos rendben vannak, a józan paraszti eszem nehezen veszi be: ez nem egy profitorientált magánvállalat által elvégeztetett vizsgálat, hanem egy állami, 100%-ban közpénzből finanszírozott kutatás. Ha úgy tetszik, a megrendelője a magyar nemzet. Hallott már valaki olyat, hogy a megrendelő nem olvashatja el az általa megrendelt kutatás tervét?! Ezt a kutatást az utolsó fillérig a magyar adófizetők finanszírozzák, azt gondolnám, hogy magyarázatot sem igényel, hogy akkor el is olvashatják, hogy mit fizetnek. Ez csak hatványozottan igaz jelen helyzetben, ahol kiemelt közérdek fűződik ahhoz is, hogy a kutatás a legjobb színvonalú legyen, és ahhoz is, hogy a közbizalom teljes legyen a vizsgálatot illetően.
A legmeredekebb egyébként, hogy manapság már egy sor profitorientált magánvállalat is nyilvánosan közzéteszi a gyógyszervizsgálataik teljes terjedelmű protokollját; komplett újság létezik, ami semmi mást nem csinál, csak ilyen protokollokat közöl. Ez az újság mára már külön rovatot nyitott a koronavírussal kapcsolatos klinikai kutatások protokolljainak közlésére, többek között pakisztáni, iráni, szudáni vizsgálatok protokolljaival. Szomorú ezt leírni, de a jelek szerint a magyar kutatást megtervezők úgy vélekednek, hogy hazájuk lakossága még nem tart ott, mint ezen országoké, hogy elérhetővé lehetne tenni számukra a kutatás protokollját.
Első probléma: a vizsgálatban nincs kontrollcsoport
Erre nehéz higgadtan bármit mondani, felfoghatatlan, hogy hogyan lehetett a vizsgálatot így megtervezni és engedélyezni, de nagyon úgy néz ki, hogy a vizsgálatban nincs kontrollcsoport! Minden résztvevő kap gyógyszert, így viszont az eredményeiket egyszerűen nem lesz mihez hasonlítani. Ha ki is derül a vizsgálatból a példa kedvéért (és tényleg csak példa kedvéért, mert ilyen nem igazán tud kiderülni a kutatásból – de erről picit később), hogy a gyógyszerrel kezelt betegek 10%-a halt meg adott időn belül, fogalmunk sem lesz, hogy ez mit jelent. Ez most jó? Vagy rossz? Mihez képest sok vagy kevés? Működött-e a gyógyszer? Elképzelésünk sem lehet, hiszen ahhoz tudni kellene, hogy mi történt volna kezelés híján! Ha 20% halt volna meg gyógyszeres kezelés nélkül, akkor nagyon is hatott a gyógyszer, ha 10, akkor nem ért semmit, ha 5, akkor még ártott is. Önmagában attól, hogy 10% halt meg, a három eset bármelyike fennállhat.
Az ember első gondolata, hogy akkor hasonlítsuk a halálozási arányt az országos adatokhoz, vagy a korábbi tapasztalatokhoz – elvégre ezekben szintén remdesivirrel nem kezelt betegek vannak, és nekünk most pont arra van szükségünk, hogy a körükben mennyi a halálozás, nem? Az ilyen megközelítésekkel az a baj, hogy nem fogjuk tudni, hogy az összehasonlítási alapot képező betegek az egyéb jellemzőikben hogyan viszonyulnak a gyógyszervizsgálatban szereplő betegekhez. Mi van, ha fiatalabbak? Vagy pont idősebbek? Mi van, ha több, vagy épp kevesebb köztük a férfi? Mi van, ha más a cukorbetegek, asztmások, vagy bármilyen más társbetegségben szenvedők aránya? Ezek mind hatnak a gyógyulási esélyekre. Úgyhogy meg vagyunk lőve: lehet, hogy a korábbi tapasztalatok szerint 5% hal meg, a gyógyszerrel kezeltek között pedig 10, de a gyógyszer mégis hatásos, mert a gyógyszervizsgálatban résztvevők mondjuk sokkal idősebbek átlagban. Vagy pont fordítva: 5% hal meg gyógyszerrel, míg az országos adatok szerint 10, de a gyógyszer mégis hatástalan, mert a gyógyszervizsgálatban jóval kisebb volt a szív-érrendszeri betegségben szenvedők aránya. Az ilyen problémákon statisztikai úton lehet ugyan javítani, de ezeket a megközelítéseket korlátozza, hogy csak azokat az eltéréseket tudjuk kiküszöbölni – és azokat sem tökéletesen – amikről eszünkbe jut, hogy ilyen gondot okozhatnak, és amikről tudunk adatot szerezni.
Pontosan ez az oka annak, hogy a valódi klinikai vizsgálatokban azt csinálják, hogy a bevont betegeket két csoportra osztják, mégpedig – és ez nagyon fontos! – véletlenszerűen, és a két csoportot hasonlítják egymáshoz. Ilyen módon garantálható, hogy nem lesz szisztematikus különbség a csoportok között életkori összetételben, nemi összetételben, társbetegségek szerint, sem semmilyen tényezőben – azokban sem, amikről nincs információnk! (Persze egy sor apróságra oda kell figyelni, például hogy ha úgy döntünk, hogy a kontrollcsoport nem kap gyógyszert – ez elfogadható lehet, ha a betegségre nincs ismerten hatásos és biztonságos szer – akkor ők a vizsgált gyógyszerrel mindenben azonos, de hatóanyagot nem tartalmazó placebót kapjanak, hogy senki ne tudhassa, hogy melyik csoportban van, és így a kezelésben részesülés tudatában se legyen eltérés stb.)
Természetesen nem ez lenne a történelem első nem kontrollált vizsgálata, de látni kell, hogy ez az egyetlen kutatás-tervezői döntés önmagában a töredékére csökkenti az egész vizsgálat bizonyító erejét – bármi is jöjjön ki belőle.
Második probléma: a kutatás azt vizsgálja elsősorban, amit eleve is tudunk, és azt csak másodsorban, ami a legérdekesebb lenne
Egy klinikai vizsgálat végpontjának szokás nevezni a kimenetet, amin lemérjük gyógyszer hatásosságát vagy biztonságosságát. Ezek közül az elsődleges végpontok azok, amelyek kiemelten fontosak, és amelyek alapján tervezzük a kutatás mintanagyságát (vagyis a bevont betegek számát). Másodlagos végpont minden egyéb, amit feljegyzésre érdemesnek találunk, de kevésbé lényeges a kutatás tervezésében, és nem alapja a betegszám meghatározásának. A másodlagos végpontok mindig kiegészítő jellegűek, és a belőlük származó eredményeket óvatosabban, több fenntartással kell értékelni.
A magyar vizsgálatnak egyetlen elsődleges végpontja van: a súlyos, gyógyszer okozta mellékhatás (halál, nagyon súlyos allergiás reakció, akut légzési elégtelenség stb.) előfordulása.
És pont.
A magyar vizsgálat elsődleges végpontként semmi mást nem vizsgál, kizárólag azt, hogy mellékhatása lesz-e az embernek a gyógyszertől. Pontosabban szólva abból is csak a súlyosat keresi, hatásosságról pedig még csak szó sincs. Tehát bár például a halál is szerepel az előbbi listában, de ez nem azt jelenti, hogy hányan haltak meg, itt kizárólag azt számolják, hogy a gyógyszer miatt hányan haltak meg. Ami jó eséllyel, és ami még fontosabb, előre megmondható módon, nulla vagy közel nulla százaléka lesz a kezelteknek.
Az ugyanis, hogy maga a gyógyszer nem öli meg a betegeket, eddig is elég biztosan tudható volt, hiszen összességében, ha nem is feltétlenül koronavírus ellen, de azért elég sokan kaptak már remdesivirt. Az azért feltűnt volna, ha halomra halnak a betegek (mármint magától a gyógyszertől), és nem túl valószínű, hogy ebben eltérés lenne a magyar betegek és a világ többi részéről származó betegek között. (A már említett amerikai vizsgálatban a remdesivirt kapó nagyjából 500 beteg közül hétnek lett súlyos mellékhatása a szertől, egynek életet fenyegető, és senki nem halt meg tőle.) Persze, nem mondom, hogy nem kell ezt is nyomon követni, dehogynem kell, rakjuk be egy jó kis másodlagos végpontnak. Na de mi legyen az elsődleges végpont? Nyilván a gyógyszer hatásossága, hiszen az az igazi, húsbavágó, nyitott kérdés. Ez azonban a hazai vizsgálatban csak másodlagos végpont.
Hangsúlyozom, a „megerősítő biztonságossági” vizsgálattal – ahová ez a magyar kutatás is tartozik – önmagában semmi baj nincs, teljesen legitim vizsgálati forma. Nem arról van szó, hogy egy ilyen vizsgálat értelmetlen. A kérdés az, hogy a szűkösen rendelkezésre álló pénzt, vizsgálati kapacitást (bevonható beteget, vizsgáló orvost, időt stb.) miért annak a még biztosabb megerősítésére használja az ország, amit vizsgálat nélkül is a legbiztosabban tudunk, és miért azt vizsgáljuk másodlagosan, ami a legfontosabb kérdés lenne, mert a legkevésbé biztosan tudjuk?
(Zárójelben teszem hozzá, hogy ez a probléma nem független az előző problémától: mivel nincs kontrollcsoport, valójában még a biztonságról sem lesz igazán megbízható adatunk. Ha ugyanis a mellékhatás nem rendelhető egyértelműen hozzá a gyógyszerhez orvosi megfontolások alapján, akkor az egyedüli módszerünk eldönteni, hogy azt a gyógyszer okozta-e, az, ha megnézzük, hogy szignifikánsan gyakoribb-e a kezelt csoportban, mint a kontrollcsoportban. Csakhogy itt ugyebár nincs is kontrollcsoport.)
Harmadik probléma: 10 hónap elteltével értékelnek ki dolgokat, amik már pár hét után ismertek
A vizsgálatban a végpontokat kiértékelni, tehát meghatározni, hogy melyik betegnek mi lett a kimenete adott végponton, például mekkora arányban lépett fel súlyos, gyógyszer okozta mellékhatás, 10 hónapnál fogják.
Ez számomra egyszerűen felfoghatatlan: az elsődleges végpont, és a másodlagos végpontok többsége olyan, ami a gyógyszer szedése alatt, annak időtartama során, vagy azt követően nagyon rövid időn belül tud csak bekövetkezni. (Gyógyszer mellékhatása ugyan lehet késői, a gyógyszer szedése utáni, de pont az itteni elsődleges végpontban felsorolt mellékhatások mind kifejezetten akut jellegűek. Anafilaxia – súlyos, gyorsan jelentkező allergiás reakció – például nem tud fél évvel a gyógyszer bevétele után fellépni.)
A gyógyszert az alkalmazási előirata szerint 5, legfeljebb 10 napig lehet adni, azaz ezek a dolgok – némi ráhagyással – mondjuk 1 hónapon belül biztosan ismertek lesznek. Miért várnak 10 hónapot a kiértékeléssel?! A legszebb, hogy a másodlagos végpontok között olyan is van, hogy „láz megszűnése az utolsó adag beadását követő 14 napon belül”, tehát itt matematikailag garantált, hogy 28 nap múlva ismert kell legyen az eredmény – de ezt is csak 10 hónapnál értékelik ki! Nem értem, hogy ez hogyan kapott így engedélyt (vagy egyszerűen elgépelték ezt a rovatot?).
Mindez teljesen értelmetlen módon késlelteti a nyert információk megismerését. Elvileg így csak akkor lesz végeredménye a vizsgálatnak, amikor az utolsó beteg bevonása után is eltelt 10 hónap, amire semmilyen racionális magyarázatot nem tudtam találni.
Az is érdekes, hogy mindeközben a vizsgálat vezetői már néhány nap után nyilatkoztak a sajtónak az eredményekről, elmondva, hogy a betegek körében eddig nem lépett fel súlyos mellékhatás (ahogy az nagyjából előre is tudható volt). Az, hogy a kutatás lezárása előtt is közölnek információt, nem feltétlenül ördögtől való, sok vizsgálat meghatározza, hogy menet közben is végeznek ún. interim kiértékelést; remélhetőleg ezek a nyilatkozatok is ilyen, előre meghatározott és a protokollban specifikált interim analízis elvégzésén nyugszanak. Ami izgalmasabb, hogy ha így van, és készült interim kiértékelés, akkor miért nem mondanak semmit a másodlagos végpontokról, a hatásosságról, azaz pont arról, ami az igazán érdekes lenne? Eltekintve persze attól, hogy kontrollcsoport híján ezt nem igazán lehet majd megítélni…
Konklúzió
Nem látok a vizsgálatot megtervezők és engedélyezők fejébe, így elképzelésem sincs, hogy vajon miért így tervezték meg ezt a vizsgálatot, de hogy ebből ilyen formában nem fogunk érdemi új tudományos információt nyerni, az biztos. Ha ebben igazam van, komoly etikai kérdéseket vet fel, hogy 2000 beteget akarnak egy ilyen kutatásba bevonni.
Etikailag nagyon aggályosnak érzem azt is, hogy a vizsgálatban részt vevő orvosok közben olyan nyilatkozatokat tesznek a médiában mint, hogy „a klinikai vizsgálatot folytatjuk, éppen azért, hogy a kontrollált körülmények között történő vizsgálat tudományosan igazolhassa, valójában mennyire hatékony a remdesivir” vagy, hogy csak a klinikai vizsgálat végén „lehet kijelenteni, hogy hatékony vagy nem hatékony [a remdesivir]”. (Előbbit a Semmelweis Egyetem Pulmonológiai Klinikájának igazgatója, utóbbit a László Kórház osztályvezetője mondta – de nem a személy a lényeg, hanem a jelenség.)
Mint láttuk, gyakorlatilag borítékolható, hogy a hatékonyságról a világon semmit nem fogunk megtudni. A legdurvább, hogy ráadásul ez deklaráltan is így van: a vizsgálat gyógyszerhatósághoz leadott hivatalos elnevezése az, hogy „kutatás a remdesivir biztonságosságának felmérésére” („study to assess the safety of remdesivir”). Még egyszer: ez az általuk választott hivatalos név! Akkor miért kell olyat mondani a sajtónak, hogy azt vizsgáljuk, hogy mennyire hatékony a remdesivir?! Az se jó, ha azért mondanak ilyet, mert azt sem tudják, hogy mi történik a vizsgálatban, a másik lehetőségbe pedig bele sem szeretnék gondolni.
Itt tehát többről van szó, mint egy elszalasztott lehetőségről. Mint azt az előbbi nyilatkozatok is mutatják, az ország közvéleményét abban a hiszemben tartják, hogy a vizsgálatból érdemi új információkat fogunk megtudni a gyógyszerről. Még rosszabb, hogy a résztvevő betegeket is minden bizonnyal erre hivatkozva vonták be a vizsgálatba. Az, hogy csalatkozniuk kell, alkalmas arra, hogy aláássa a bizalmat a gyógyszerben, rosszabb esetben aláássa a bizalmat a magyar klinikai vizsgálatokban általában, legrosszabb esetben pedig a járvány elleni védekezést is gyengítheti.
